第一作者:左洪娜、吴爱伟
通讯作者:汪虎
发表期刊:Nature Communications
期刊 5-Year Impact Factor: 16.1
通讯单位:杭州师范大学基础医学院
论文DOI :https://doi.org/10.1038/s41467-024-50110-9
成果简介
骨髓中的造血干细胞(HSCs)具有长期自我更新和多谱系分化能力,对整个生命过程中血液细胞的生产至关重要。HSCs具有强大的适应能力以维持干细胞功能并应对各种内外部压力,但其机制尚未完全阐明。HSCs从静息状态激活,经历克隆扩增和分化,此过程需通过上调蛋白质合成实现大量能量和生物合成,其中mTOR通路扮演核心角色。mTOR活性对于维持HSCs至关重要;其过度激活或抑制均影响干细胞活性。tRNAs的化学修饰,特别是N1-甲基腺苷(m1A)修饰,影响翻译效率,而甲基转移酶TRMT6/TRMT61A介导的m1A58修饰可增强翻译起始和延伸。最近有研究报道,过表达TRMT6-TRMT61A复合体以不依赖tRNA-m1A58修饰的作用促进HSC老化。除此之外,TRMT6/TRMT61A在HSCs中的体内生物学功能仍然完全未知。
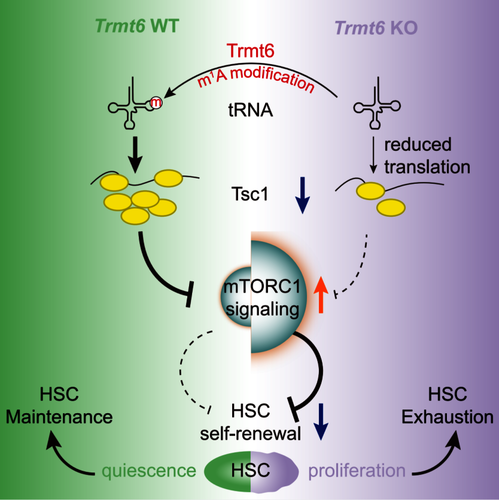
2024年7月8日,杭州师范大学基础医学院汪虎团队在Nature Communications在线发表了题为“tRNA m1A modification regulate HSC maintenance and self-renewal via mTORC1 signaling”的研究论文。该研究发现TRMT6/TRMT61A介导的tRNA-m1A58修饰通过控制TSC1的翻译对mTOR通路发挥关键调控作用,是维持HSCs稳态和功能的重要机制。
在该研究中,作者发现特异性敲除Trmt6导致HSC短暂异常扩增,在竞争性移植实验中,TRMT6缺乏的HSCs表现出自我更新能力受损。作者对其机制进行探索,单细胞RNA-seq分析揭示,在Trmt6基因缺失后,HSCs中mTORC1信号通路高度上调。m1A-tRNA-seq和Western blot分析表明,TRMT6促进特定tRNA的m1A修饰和TSC1的表达,从而精细调节mTORC1信号水平。此外,雷帕霉素对mTORC1通路的抑制挽救了TRMT6缺乏HSCs的功能缺陷。总之,本研究阐明了TRMT6-tRNA m1A-TSC1-mTORC1调控轴在调控HSC稳态和功能中的关键作用,为深入理解干细胞功能和调控提供了新视角。
作者简介
通讯作者 汪虎
基础医学院教授,科研处副处长;国家“优青”获得者,入选省万人计划。研究方向为干细胞衰老的机制和应用,第一或通讯作者在领域内权威期刊 Cell Stem Cell,Cell Research,Nature communications,Blood等发表 SCI论文30余篇。 先后主持多项国家级项目,包括:国家重点研发计划干细胞及转化研究重点专项项目课题、国家自然科学基金优秀青年基金项目、衰老重大研究计划集成项目子课题和培育项目、国自然面上项目和青年项目等。现任浙江大学生命科学学院兼任教授,浙江大学附属第一医院全国重点实验室PI,杭师大附属医院心血管科双聘教授。中国老年医学学会委员,中国生物物理学学会衰老生物学分会委员,国际血液学学会(ISEH)会员,Biophysics Reports青年编委等。