学术成果一
第一作者:梁千、徐诗雯
通讯作者:丛羽生、李国庆
发表期刊:Redox Biology
期刊5-Year Impact Factor:13.1
通讯单位:杭州师范大学、南华大学
论文DOI:https://doi.org/10.1016/j.redox.2026.104046
学术成果二
第一作者:方瑶瑶
通讯作者:丛羽生、梁千
发表期刊:Journal of Biological Chemistry
期刊5-Year Impact Factor:4.3
通讯单位:杭州师范大学
论文DOI:https://doi.org/10.1016/j.jbc.2026.111320
基础医学院丛羽生教授团队近期在蛋白质犹素化修饰(UFMylation)研究领域取得新进展,相关成果相继发表于国际知名期刊 Redox Biology(2026, 90:104046)与 Journal of Biological Chemistry(2026, 302 (4):111320)。团队不仅建立了一套高效、特异的修饰研究技术体系,为底物筛选与机制探索提供了全新工具,揭示了犹素化修饰缺陷通过调控KEAP1-NRF2通路促进肝细胞癌发生的分子机制,为该肿瘤的靶向治疗提供了新的理论依据与潜在靶点。
犹素化修饰是一类重要的类泛素化翻译后修饰,通过UBA5(E1)、UFC1(E2)及UFL1/DDRGK1/CDK5RAP3(E3)构成的酶促级联反应,将UFM1共价连接至底物蛋白的赖氨酸残基上。该修饰参与调控细胞分化、内质网稳态、DNA损伤修复等多种生理过程,其失调与癌症、发育障碍等多种疾病密切相关。修饰缺陷可导致小鼠胚胎致死,显示出重要的生物学功能。然而,目前已知的犹素化修饰底物不足30个,其具体分子机制、底物谱及所调控的细胞信号网络仍知之甚少。长期以来,该领域面临两大技术瓶颈:一是高丰度底物的修饰信号容易掩盖低丰度底物,检测难度大;二是传统方法多依赖过表达修饰酶来提升修饰水平,操作繁琐且特异性低。
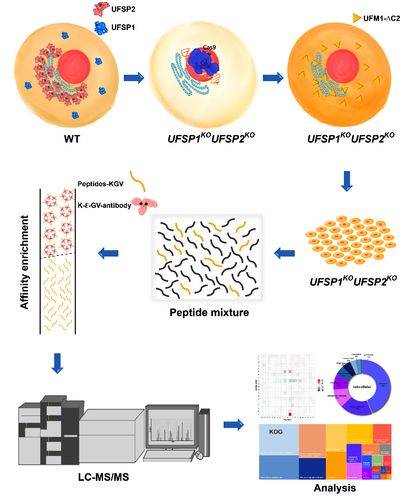
针对上述难点,丛羽生教授团队在修饰研究技术方面开展了系统性优化,成果应邀发表于Cell子刊(STAR Protocols,2022)。2022年,团队梁千博士发现人源UFSP1可通过上游“近同源启动子(CUG)”起始翻译,产生具有完整催化活性和底物特异性的犹素化修饰蛋白酶,该成果发表于 Journal of Biological Chemistry 杂志并入选该刊Editors' Picks(jbc.2022.102016)。在此基础上,梁千博士进一步构建了犹素化修饰完全阻断的UFSP1/UFSP2双基因敲除(DKO)人源HEK293T细胞株。 2026年,团队利用该细胞株建立了 “双敲除细胞系 + 核心酶共表达 + 特异性抗体富集 + LC-MS/MS” 的全新技术体系,实现了底物的大规模高效鉴定,共鉴定出超过600个候选底物,极大丰富了犹素化修饰底物库,该成果再次发表于Journal of Biological Chemistry(2026)。通过系统的生物信息学分析,研究明确了犹素化修饰的氨基酸偏好性、底物亚细胞定位特征及主要参与的细胞通路,为修饰位点预测工具的开发奠定了基础,也为解析其生物学功能提供了重要的数据资源。该技术体系突破了该领域长期存在的技术瓶颈,为相关研究提供了高效可靠的工具,具有重要的方法学价值。
犹素化修饰底物鉴定策略图
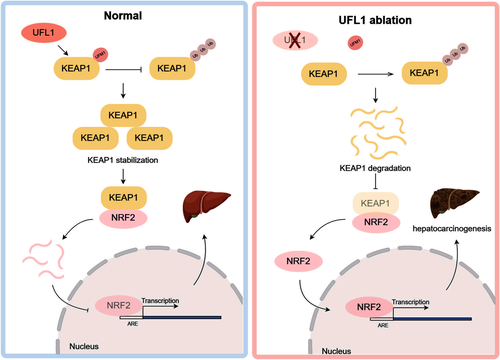
团队近期将犹素化修饰研究与肝脏疾病相结合,利用生物化学、分子细胞生物学、多组学技术、临床数据及基因编辑小鼠模型,系统探索了该修饰在肝脏中的功能机制。近期发表于 Redox Biology 的研究中,团队构建了肝细胞特异性Ufl1基因敲除小鼠模型,发现Ufl1缺失可导致明显的肝脏病理损伤,包括肝细胞肿大、脂肪变性、炎症浸润和肝纤维化,血清肝损伤标志物显著升高,且小鼠对二乙基亚硝胺(DEN)诱导的肝癌易感性显著增加。20月龄的敲除小鼠更出现自发性肝癌,证实UFL1缺失是肝癌发生的重要危险因素。通过转录组测序与功能验证,研究鉴定KEAP1为犹素化修饰的新底物,修饰位点定位于赖氨酸残基K131。机制研究表明,UFL1介导的犹素化修饰通过拮抗泛素化降解维持KEAP1蛋白稳定性;当修饰缺陷时,KEAP1发生泛素化降解,对NRF2的负调控作用丧失,导致NRF2在细胞核内大量累积并异常激活下游靶基因,最终通过KEAP1-NRF2通路的过度激活促进肝细胞恶性转化。临床样本分析进一步证实,人肝癌组织中UFL1与KEAP1表达均显著降低且呈正相关,而NRF2表达显著升高;UFL1或KEAP1低表达与肝癌患者不良预后密切相关,提示UFMylation-KEAP1-NRF2通路在肝癌发生中具有重要作用及潜在治疗靶点。
犹素化修饰调控KEAP-NRF2通路在肝癌发生中的作用机制
近年来,丛羽生教授团队聚焦犹素化修饰的生物学功能与机制研究,已在 Nature Cell Biology、Nature Communications、PNAS、Nucleic Acids Research、Nature Structural & Molecular Biology等国际期刊发表系列文章。相关工作获得国家自然科学基金重点项目及联合基金重点项目、浙江省科技厅、杭州师范大学交叉学科研究项目等多项资助。未来,团队将进一步系统探索犹素化修饰在细胞稳态、组织器官生理病理及疾病发生发展中的作用与分子机制,以期为转化医学与临床诊治策略提供科学依据。